Fosforescenca je luminiscenca, ki se pojavi ko energija dobavlja ga elektromagnetno sevanje, ponavadi ultravijolična svetloba. Vir energije brca elektron atom iz nižje energijskega stanja v "vznemirjeno" višje energijsko stanje; potem elektron sprosti energijo v obliki vidna svetloba (luminiscenca), ko pade nazaj v nižje energijsko stanje.
Ključni odvzemi: fosforescenca
- Fosforescenca je vrsta fotoluminiscence.
- V fosforescenci svetloba absorbira material, ki dviguje energijske ravni elektronov v vznemirjeno stanje. Vendar se energija svetlobe ne ujema povsem z energijo dovoljenih vznemirjenih stanj, zato se absorbirane fotografije zataknejo v trojno stanje. Prehodi v nižje in stabilnejše energijsko stanje potrebujejo čas, ko pa se pojavijo, se sprosti svetloba. Ker se to sproščanje pojavlja počasi, se zdi, da fosforescenten material sveti v temi.
- Primeri fosforescentnih materialov vključujejo svetleče se temne zvezde, nekatere varnostne znake in žareče barve. Za razliko od fosforescentnih izdelkov fluorescenčni pigmenti prenehajo žareti, ko se svetlobni vir odstrani.
- Čeprav je poimenovan po zelenem sijaju elementa fosfor, fosfor pravzaprav sveti zaradi oksidacije. Ni fosforrescentno!
Preprosta razlaga
Fosforescenca počasi sprošča shranjeno energijo. V osnovi fosforescentni material "napolnimo" tako, da ga izpostavimo svetlobi. Potem se energija shrani za nekaj časa in se počasi sprosti. Ko se energija sprosti takoj po absorpciji vpadne energije, se pokliče postopek fluorescenca.
Pojasnilo kvantne mehanike
V fluorescenci površina absorbira in ponovno oddaja foton skoraj v trenutku (približno 10 nanosekund). Fotoluminiscenca je hitra, saj se energija absorbiranih fotonov ujema z energijskimi stanji in dovoljenimi prehodi materiala. Fosforescenca traja veliko dlje (milisekunde do dni), ker absorbirani elektron prestopi v vznemirjeno stanje z večjo spin množino. Navdušeni elektroni se ujamejo v trojno stanje in lahko uporabijo le "prepovedane" prehode, da se spustijo v nižje energijsko singletno stanje. Kvantna mehanika omogoča prepovedan prehod, vendar niso kinetično ugodni, zato trajajo dlje. Če absorbiramo dovolj svetlobe, shranjena in sproščena svetloba postane dovolj pomembna, da se lahko v materialu svetijo temno. "Zaradi tega se fosforescentni materiali, kot fluorescenčni materiali, pod črno (ultravijolično) svetlobo zdijo zelo svetli. Jablonski diagram se običajno uporablja za prikaz razlike med fluorescenco in fosforescenco.
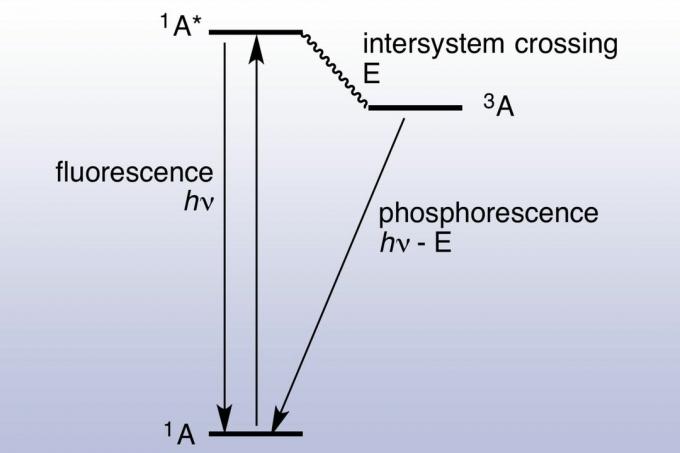
Zgodovina
Študija fosforescentnih materialov sega vsaj v leto 1602, ko je Italijan Vincenzo Casciarolo opisal "lapis solaris" (sončni kamen) ali "lapis lunaris" (lunin kamen). Odkritje je opisal profesor knjige filozofije Giulio Cesare la Galla iz leta 1612 De Phenomenis v Orbe Lunae. La Galla poroča, da je kamen Casciarolo na njem oddajal svetlobo, potem ko se je s segrevanjem kalcificiral. Dobila je svetlobo od Sonca in nato (kot Luna) oddajala svetlobo v temi. Kamen je bil nečist barit, čeprav tudi drugi minerali kažejo fosforescenco. Vključujejo nekatere diamanti (znan indijskemu kralju Bhoji že 1010–1055, ponovno ga je odkril Albertus Magnus in ga ponovno odkril Robert Boyle) in beli topaz. Kitajci so zlasti cenili vrsto fluorita, imenovanega klorofan, ki bi prikazoval luminiscenco zaradi telesne toplote, izpostavljenosti svetlobi ali drgnjenju. Zanimanje za naravo fosforescentnosti in druge vrste luminescence je na koncu pripeljalo do odkritja radioaktivnosti leta 1896.
Materiali
Poleg nekaj naravnih mineralov fosforescenco proizvajajo tudi kemične spojine. Verjetno najbolj znan od teh je cinkov sulfid, ki se v izdelkih uporablja že od tridesetih let prejšnjega stoletja. Cinkov sulfid ponavadi oddaja zeleno fosforescenco, čeprav se za spremembo barve svetlobe lahko doda fosfor. Fosfor absorbira svetlobo, ki jo oddaja fosforescenca, in jo nato sprosti kot drugo barvo.
V zadnjem času se za fosforescenco uporablja stroncijev aluminat. Ta spojina sveti desetkrat svetleje od cinkovega sulfida in tudi shrani svojo energijo veliko dlje.
Primeri fosforescence
Pogosti primeri fosforescije vključujejo zvezde, ki so jih obesili na stene spalnice, ki svetijo ure po ugasnitvi luči in barve, ki se uporabljajo za izdelavo žarečih zvezdov. Čeprav element fosfor sveti zeleno, svetloba se sprošča od oksidacije (kemiluminiscenca) in je ne primer fosforescence.
Viri
- Franz, Karl A.; Kehr, Wolfgang G.; Siggel, Alfred; Wieczoreck, Jürgen; Adam, Waldemar (2002). "Luminescentni materiali" v Ullmannova enciklopedija industrijske kemije. Wiley-VCH. Weinheim. doi: 10.1002 / 14356007.a15_519
- Roda, Aldo (2010). Kemiluminiscenca in bioluminiscenca: preteklost, sedanjost in prihodnost. Royal Society of Chemistry.
- Zitoun, D.; Bernaud, L.; Manteghetti, A (2009). Mikrovalovna sinteza fosforja, ki traja dolgo. J. Chem. Educ. 86. 72-75. doi: 10.1021 / ed086p72